

Next: Die Rüttelmaschine als
Up: Beispiel: die Rüttelmaschine
Previous: Beispiel: die Rüttelmaschine
Der zweite Hauptsatz der Thermodynamik besagt, daß die Entropie
in einem abgeschlossenen System nie abnehmen kann, daß also
keine Ordnung entstehen kann.
Der Satz wird abgeleitet mit Hilfe der Wahrscheinlichkeitsrechnung.
Man sieht sich an, wieviele mögliche Realisierungen (Mikrozustände)
es für alle energetisch möglichen (Makro-)Zustände gibt.
Die Wahrscheinlichkeit, daß ein bestimmter (Makro-)Zustand dann
tatsächlich auftritt ist dann
proportional zu der Zahl seiner möglichen Realisierungen.
Nehmen wir an, in dem Behälter seien 100 Kugeln. Dann gibt es
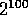 mögliche Konstellationen für die Verteilung der Kugeln auf
die beiden Seiten. Eine einzige davon repräsentiert den
Makrozustand, daß alle Kugeln links liegen und eine einzige,
daß alle Kugeln rechts liegen. Etwa
mögliche Konstellationen für die Verteilung der Kugeln auf
die beiden Seiten. Eine einzige davon repräsentiert den
Makrozustand, daß alle Kugeln links liegen und eine einzige,
daß alle Kugeln rechts liegen. Etwa 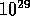 Realisierungen gibt es aber
für die fifty-fifty-Verteilung. Es ist also extrem unwahrscheinlich,
daß alle Kugeln auf einer Seite zu liegen kommen.
In der Tat kann man eine Gleichverteilung bekommen, wenn man die
Platte zunächst stark anregt und dann abrupt abschaltet.
Realisierungen gibt es aber
für die fifty-fifty-Verteilung. Es ist also extrem unwahrscheinlich,
daß alle Kugeln auf einer Seite zu liegen kommen.
In der Tat kann man eine Gleichverteilung bekommen, wenn man die
Platte zunächst stark anregt und dann abrupt abschaltet.
Regelt man die Rüttelstärke aber sehr langsam zurück, sammeln
sich alle Kugeln auf einer Seite. Auf welcher ist zufällig
(also sensitiv abhängig von Anfangsbedingungen),
wenn die Maschine symmetrisch gebaut ist und waagerecht steht.
Spontan hat sich eine Struktur gebildet, die Symmetrie wurde
gebrochen. Das ist kein Widerspruch zum zweiten Hauptsatz, weil
es sich hier nicht um ein geschlossenes System handelt und
die Entropie in der Nähe des Kraftwerks, das den Strom für
die Maschine produziert, steigt.
Werner Eberl
Sat Apr 15 13:17:50 MET DST 1995
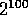 mögliche Konstellationen für die Verteilung der Kugeln auf
die beiden Seiten. Eine einzige davon repräsentiert den
Makrozustand, daß alle Kugeln links liegen und eine einzige,
daß alle Kugeln rechts liegen. Etwa
mögliche Konstellationen für die Verteilung der Kugeln auf
die beiden Seiten. Eine einzige davon repräsentiert den
Makrozustand, daß alle Kugeln links liegen und eine einzige,
daß alle Kugeln rechts liegen. Etwa 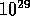 Realisierungen gibt es aber
für die fifty-fifty-Verteilung. Es ist also extrem unwahrscheinlich,
daß alle Kugeln auf einer Seite zu liegen kommen.
In der Tat kann man eine Gleichverteilung bekommen, wenn man die
Platte zunächst stark anregt und dann abrupt abschaltet.
Realisierungen gibt es aber
für die fifty-fifty-Verteilung. Es ist also extrem unwahrscheinlich,
daß alle Kugeln auf einer Seite zu liegen kommen.
In der Tat kann man eine Gleichverteilung bekommen, wenn man die
Platte zunächst stark anregt und dann abrupt abschaltet.